Клеточная терапия нейродегенеративных заболеваний AMBROSE
Благодаря десятилетиям исследований наше понимание нейродегенеративных заболеваний заметно расширилось. Были установлены более четкие связи между некоторыми ключевыми факторами, присутствующими у пациентов, перенесших травматическое повреждение мозга или страдающих такими заболеваниями, как деменция, болезнь Альцгеймера или болезнь Паркинсона.
В последние годы воспаление все чаще рассматривается как часть причина нейродегенерации, а не просто быть ее результатом. Эти важные открытия, опубликованные в научной литературе, изменили наше представление о заболеваниях мозга и, следовательно, о способах их лечения.
Системное воспаление и когнитивный спад
Системное воспаление является общим фактором болезней старения - оно охватывает широкий спектр тяжелых, изнурительных, а иногда и опасных для жизни состояний.[1] Ученые, исследующие заболевания головного мозга, сегодня широко признают, что широко распространенное воспаление вовлечено в пагубный процесс болезни Паркинсона[2] а также деменцию и, в частности, ее наиболее распространенную форму - болезнь Альцгеймера (БА).[3]
Информативное исследование, проведенное в 2009 году, установило тесную связь между уровнем воспаления и симптомами болезни. 300 пациентов с легкой и тяжелой формой болезни Альцгеймера с помощью ухаживающих за ними лиц оценили исходный уровень когнитивных функций и проверили уровень молекулы (цитокина), вызывающей воспаление (провоспалительный процесс), под названием фактор некроза опухоли-альфа (TNF-a).
Затем исследователи фиксировали любое новое острое системное воспалительное событие, например, болезнь или физическую травму, произошедшее после первоначального тестирования, и повторно проверяли когнитивные функции и уровень TNF-a через 2, 4 и 6 месяцев, чтобы сравнить с исходным уровнем, отмеченным в начале исследования. В итоге выяснилось, что как острое, так и хроническое системное воспаление, измеряемое повышением уровня провоспалительного TNF-a, довольно сильно коррелирует с увеличением когнитивного спада у пациентов, участвовавших в исследовании.[4]
Воспалительно-иммунный ответ
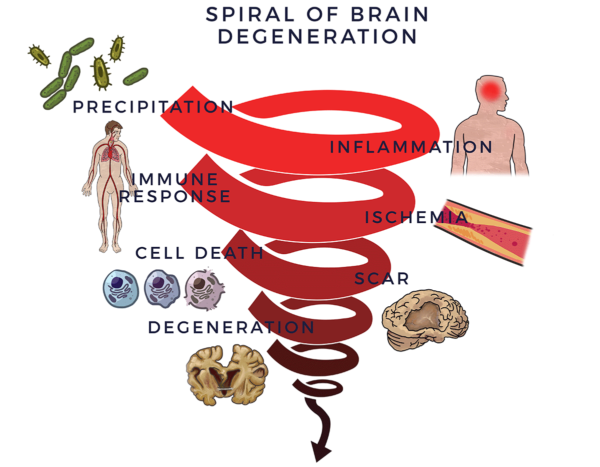
Неврологическая дисфункция начинается с пускового механизма, такого как травма (например, бокс или другая черепно-мозговая травма), инсульт, инфекция, выбор образа жизни (например, курение), токсины окружающей среды, наследственные факторы или их сочетание. Один или несколько из этих факторов приводят к нейровоспалению[5]Определяется как хроническое и постоянное воспаление в центральной нервной системе (ЦНС) и головном мозге.
Чтобы защитить мозг, иммунная система запускает ответную реакцию. Когда этот процесс выходит из-под контроля, иммунный ответ становится равносильным тому, как если бы у вас на заднем сиденье сидел водитель, который хронически неадекватно реагирует, "помогая" вам управлять автомобилем. Это также называется воспалительно-иммунным ответом и приводит к снижению кровотока (ишемии) в мозге. Без хорошего кровообращения, доставляющего кислород и необходимые питательные вещества для поддержания здоровья мозга[6]Нервные клетки отмирают. Шрамы, бляшки или белки заменяют здоровые ткани, и мозг деградирует. Мы называем этот процесс спиралью дегенерации.
Потеря нейронов (нервных клеток) влияет на равновесие, движения, речь, дыхание и память по-разному и в разные моменты времени в зависимости от конкретного диагноза и скорости ухудшения состояния. Болезнь Паркинсона связана с потерей нервных клеток, которые вырабатывают в мозге химическое вещество дофамин. Недостаток дофамина вызывает тремор, нарушения равновесия, движения и речи. Это также может привести к депрессии и ухудшению памяти.
Все чаще признается, что факторы спирали приводят к появлению симптомов и ухудшению повседневной жизни, которые являются следствием заболеваний, связанных с головным мозгом. [7] [8] [9]
Мозг - невероятно живучий орган. К тому времени, когда такое состояние, как болезнь Паркинсона или деменция (и связанные с ними амилоидные бляшки, белки тау или тельца Леви), становится очевидным, они могут развиваться в течение десятилетия или более в прогрессивно ухудшающейся последовательности событий.
Процесс ремонта
Благодаря механизму межклеточной коммуникации, известному как паракринная сигнализация[10]Стволовые и регенеративные клетки, полученные из жировой ткани (ADRCs), мобилизуют близлежащие клетки для более эффективной работы.
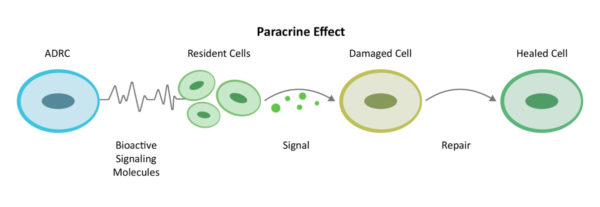
ADRC также активируют клетки-резиденты, которые уже находятся в месте воспаления и повреждения в мозге, но спят на рабочем месте, чтобы вернуться к работе, выполняя свою роль. Эти клетки-резиденты сначала уменьшают воспаление и чрезмерно активные иммунные реакции. После того как иммунная система утихает, они усиливают кровообращение за счет роста новых кровеносных сосудов и восстанавливают здоровье существующих сосудов, предотвращают дальнейшую запрограммированную гибель клеток (апоптоз), уменьшают размер рубца и, наконец, восстанавливают здоровую ткань и нервы.
Мы называем это процессом восстановления. Таким образом организм естественным образом восстанавливается после травм, а процессы заживления поддерживаются многочисленными механизмами действия ADRCs, направленными на восстановление и регенерацию мозга, а также на контроль системного воспаления.
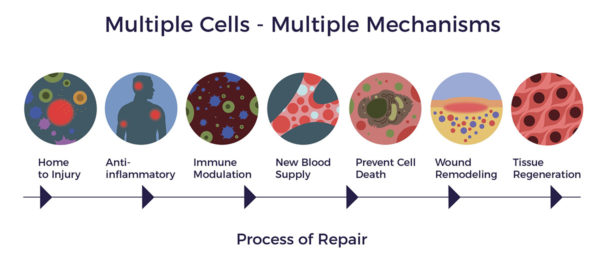
В результате многочисленных действий, которые выполняют ADRC, могут образовываться новые кровеносные сосуды и новые нейроны в мозге.[11] [12] Как показало недавнее исследование на животных, ADRC также уменьшают повреждения в мозге (как в случае инсульта или черепно-мозговой травмы) и тем самым положительно влияют на обучение и память.[13]
Несколько ячеек, несколько функций
В отличие от фармацевтических препаратов, которые полагаются на одну молекулу или химическое вещество для подавления наиболее значимого фактора болезни, как, например, множество лекарств, разработанных для борьбы с амилоидным скоплением, все из которых потерпели неудачу в клинических испытаниях, ADRC покрывают больную ткань или орган сотнями биологически активных молекул, которые способствуют восстановлению клеток, нервов и тканей, где это необходимо.[14] [15] Другими словами, мы полагаемся не на звездного игрока с определенной специализацией, а на целую команду таких же компетентных игроков.
Мезенхимальные стволовые клетки (МСК), тип стволовых клеток, содержащихся в жировой ткани, выделяют полезные химические вещества и факторы роста, которые, как известно, способствуют выживанию и регенерации нейронных клеток посредством паракринной сигнализации. Это важная функция, которая способствует различным аспектам восстановления травмированного мозга путем уменьшения гибели клеток, увеличения роста новой нервной ткани, а также формирования новых кровеносных сосудов.[16]
Важная группа биологически активных молекул, выделяемых из ADRCs, называется нейротрофическими факторами (NTFs); "нейро" означает "нерв", а "трофический" - от древнегреческого trophikós, означающего "относящийся к пище или питанию". НТФ поддерживают рост, выживание и дифференцировку как развивающихся, так и зрелых нервных клеток (нейронов). Было показано, что стволовые клетки, полученные из жировой ткани (ADSCs), выделяют нейротрофический фактор роста мозга (BDNF), который способствует заживлению нервов и росту аксонов.[17] [18] [19] [20]
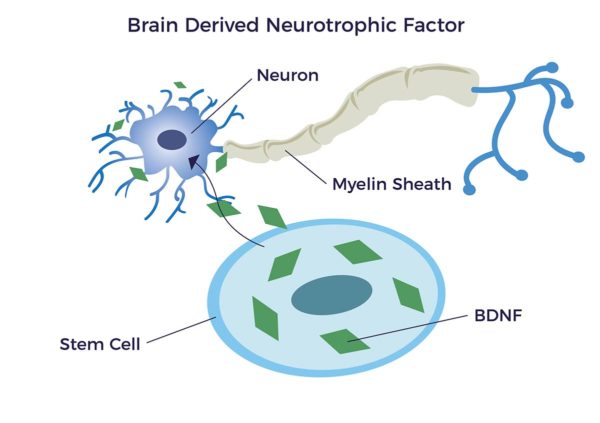 Более высокий уровень BDNF связан с повышением интеллекта, настроения, продуктивности и памяти, а также со снижением риска развития слабоумия и болезни Альцгеймера.
Более высокий уровень BDNF связан с повышением интеллекта, настроения, продуктивности и памяти, а также со снижением риска развития слабоумия и болезни Альцгеймера.
Проникновение через гематоэнцефалический барьер Гематоэнцефалический барьер
Между мозгом и внешними чужеродными веществами стоит гематоэнцефалический барьер (ГЭБ), задача которого - служить фильтром и поддерживать стабильную среду для мозга. При лечении нейродегенеративных заболеваний врачи AMBROSE вводят низкую дозу маннитола, сахарного спирта, внутривенно перед инфузией стволовых клеток. Маннитол временно открывает гематоэнцефалический барьер, благодаря чему значительно больший процент клеток может безопасно мигрировать в мозг[21] Именно его используют врачи, чтобы избавить мозг от лишней жидкости или инфекций, а также перед внутривенным введением противораковых препаратов.
Клеточная терапия AMBROSE для лечения травм головного мозга и нейродегенеративных заболеваний
Адипозные стволовые и регенеративные клетки (ADRCs) - это разнообразная популяция клеток, которые, благодаря множеству действий, способны улучшить симптомы, функции и качество жизни пациентов с заболеваниями, связанными с головным мозгом, или перенесших травматическое повреждение головного мозга.[22] [23]
Эти клетки сродни персональной пожарной, спасательной и ремонтной команде, которая естественным образом обитает в вашем теле. Они спокойно ждут сигнала о неполадках - воспаления - и затем отправляются по этому сигналу выполнять свою работу.
Используя силу собственной биологии, клеточная терапия AMBROSE представляет собой минимально инвазивный вариант для пациентов с нейродегенеративными заболеваниями, такими как болезнь Паркинсона, деменция и болезнь Альцгеймера, а также после инсульта или травматического повреждения мозга.
Пожалуйста, связаться с нами для получения дополнительной информации о лечении, кандидатах и о том, как стать пациентом.
[1] C. Franceschi and J. Campisi Chronic Inflammation (Inflammaging) and Its Potential Contribution to Age- Associated Diseases J Gerontol A Biol Sci Med Sci 2014 June;69(S1): S4-S9
[2] C. Ferrari и R. Tarelli. Болезнь Паркинсона и системное воспаление Parkinson's Dis. 2011; 2011: 436813.
[3] R Schmidt & H Schmidt et al Раннее воспаление и деменция: 25-летнее наблюдение в рамках Гонолуло-Азиатского исследования старения. 2002 Annals of neurology. 52. 168-74. 10.1002/ana.10265
[4] C. Holmes et al Системное воспаление и прогрессирование заболевания при болезни Альцгеймера Неврология® 2009; 73:768-774
[6] E Hirsch and S Hunot Нейровоспаление при болезни Паркинсона: мишень для нейропротекции? Lancet Neurol 2009; 8: 382-97
[6] Р. Н. Калария (2010). Сосудистая основа дегенерации мозга: Нестабильный контроль и факторы риска деменции. Отзывы о питании, 68(Suppl 2), S74-S87
[7] Б.В. Злокович Нейрососудистые пути развития нейродегенерации при болезни Альцгеймера и других заболеваниях. Nature reviews Neuroscience. 2011;12(12):723-738
[8] Линда Дж. Ван Элдик и др Роль воспаления и иммунных механизмов при болезни Альцгеймера Alzheimer's & Dementia: Translational Research & Clinical Interventions 2 (2016) 99-109
[9] Kim S, Chang K-A, Kim Ja, Park H-G, Ra JC, et al. (2012) Профилактические и терапевтические эффекты внутривенных человеческих адипозных стволовых клеток у мышей с болезнью Альцгеймера. PLoS ONE 7(9): e45757.
[10] A Caplan MSCs: Страж и защитники от травмы J. Cell. Physiol. 231: 1413-1416, 2016
[11] J. K. Huang et al Регенерация миелина при рассеянном склерозе: Targeting. Эндогенные стволовые клетки, Американское общество экспериментальной нейротерапии, 2011 г.
[12] A Bowles et al Иммуномодулирующие эффекты клеток стромальной фракции сосудов жировой ткани способствуют альтернативной активации макрофагов для восстановления повреждений тканей. Стволовые клетки, 2017 Aug 12
[13] Zhou F, Gao S, Wang L, et al. Стволовые клетки, полученные из жировой ткани человека, частично спасают синдромы инсульта, способствуя пространственному обучению и памяти в модели окклюзии средней мозговой артерии у мышей [опубликованная коррекция появилась в Stem Cell Res Ther. 2019 Mar 6;10(1):76]. Stem Cell Res Ther. 2015;6(1):92. Опубликовано 2015 9 мая. doi:10.1186/s13287-015-0078-1
[14] Takeshi Taksuda et al Человеческие мезенхимальные стволовые клетки, полученные из жировой ткани, выделяют функциональные экзосомы, связанные с неприлизином Scientific Reports 3: 1197
[15] A Brini et al, Терапевтический эффект человеческих адипозных стволовых клеток и их секретома при экспериментальной диабетической боли Scientific Reports 7: 9904
[16] C. Тейт и К. Кейс. Мезенхимальные стромальные клетки для лечения травмы головного мозга. Advanced Topics in Neurological Disorders.
[17] Разави, Шахназ и др. "Нейротрофические факторы и их влияние на лечение рассеянного склероза". Передовые биомедицинские исследования 4 (2015): 53. PMC. Web. 28 Sept. 2018.
[18] J. K. Huang et al Регенерация миелина при рассеянном склерозе: Targeting. Эндогенные стволовые клетки, Американское общество экспериментальной нейротерапии, 2011 г.
[19] T Lopatina et al. (2011) Стволовые клетки, полученные из жировой ткани, стимулируют регенерацию периферических нервов: BDNF, секретируемый этими клетками, способствует заживлению нервов и росту аксонов De Novo. PLoS ONE 6(3): e178991
[20] S. Seigo et al, Некультивированные регенеративные клетки, полученные из жировой ткани, способствуют регенерации периферических нервов, Journal of Orthopaedic Science, Volume 18, Issue 1, 2013, Pages 145-151
[21] C.V. Borlongan et al Проникая через гематоэнцефалический барьер и отменяя воспаление при инсульте: Implications for Stroke Therapy Curr Pharm Des. 2012; 18(25): 3670-3676
[22] Sakthiswary R, Raymond AA. Терапия стволовыми клетками при нейродегенеративных заболеваниях: От принципов к практике. Neural Regen Res. 2012;7(23):1822-1831. doi:10.3969/j.issn.1673-5374.2012.23.009
[23] Lunn JS, Sakowski SA, Hur J, Feldman EL. Технология стволовых клеток для лечения нейродегенеративных заболеваний. Ann Neurol. 2011;70(3):353–361. doi:10.1002/ana.22487