Thérapie cellulaire AMBROSE pour les maladies inflammatoires de l'intestin (MICI)
La thérapie cellulaire pour les maladies inflammatoires de l'intestin exploite la puissance des cellules souches et régénératives dérivées de l'adipeuse (ADRC) des patients. Il s'agit d'une population diversifiée de cellules qui, par le biais d'activités multiples, peuvent contribuer à améliorer les symptômes, le fonctionnement et la qualité de vie des patients souffrant de maladies telles que le syndrome du côlon irritable, la colite ulcéreuse, la maladie cœliaque et la maladie de Crohn.
Ces cellules spécialisées s'apparentent à un service "biologique" d'incendie, de secours et de réparation. Elles attendent tranquillement un signe de problème - l'inflammation - et se rendent sur place pour faire leur travail. Les scientifiques qui étudient la thérapie par cellules souches adultes pour les maladies inflammatoires de l'intestin reconnaissent aujourd'hui que les ADRC réduisent l'inflammation et rééquilibrent le système immunitaire en lançant le processus de réparation.[1] [2] [3] [4] [5]
Les maladies inflammatoires de l'intestin impliquent une inflammation chronique d'une partie du tube digestif et peuvent parfois être associées à une arthrite inflammatoire. L'arthrite de la colonne vertébrale associée aux MICI commence par une douleur lombaire subtile, en particulier chez les jeunes, et une raideur matinale. Elle s'aggrave en cas de position assise ou debout prolongée et s'améliore avec une activité modérée. Elle est plus fréquente dans la MC que dans la RCH et est indépendante des symptômes gastro-intestinaux.
Réponse inflammatoire et immunitaire
Une réponse inflammatoire peut être déclenchée par un traumatisme, une infection, des toxines environnementales, des choix de mode de vie (par exemple le tabagisme), des facteurs héréditaires ou une combinaison de ces mauvais acteurs. Ce type d'inflammation (aiguë) est essentiel à la réparation de l'organisme et est généralement de courte durée, disparaissant une fois que le processus de guérison a eu lieu.
Il existe un autre type de réaction inflammatoire persistante qui devient chronique et affecte l'ensemble de l'organisme, devenant ainsi systémique. L'inflammation systémique est un facteur commun aux maladies du vieillissement, qui couvrent un large éventail d'affections graves, débilitantes et parfois mortelles.[6]
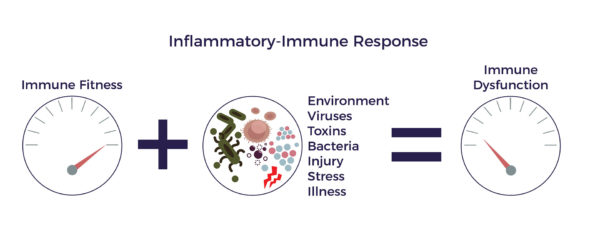
Dans le cas des maladies inflammatoires de l'intestin, l'inflammation chronique déclenche un processus vicieux préjudiciable. Elle recrute le système immunitaire, dont le rôle est de lutter contre les infections et autres processus pathologiques, pour aider à la guérison. Les cellules du système immunitaire (cellules immunitaires) sont là pour protéger l'organisme. Lorsqu'elles détectent un ennemi, elles envoient des troupes de molécules pro-inflammatoires appelées "cytokines" pour le combattre. Lorsque ce processus échappe à tout contrôle, on parle de réaction inflammatoire-immune. Cette réponse équivaut à avoir un conducteur arrière qui réagit de manière chroniquement excessive tout en vous "aidant" à conduire votre voiture. Elle entraîne ensuite une réduction de la circulation sanguine (ischémie). Sans une bonne circulation, les cellules meurent, des cicatrices se forment, les tissus et les organes dégénèrent. C'est ce que nous appelons la spirale de la dégénérescence.
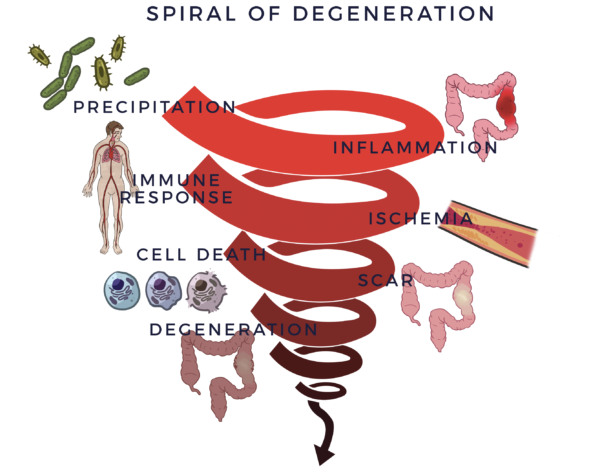
Les maladies inflammatoires de l'intestin impliquent une inflammation systémique chronique qui perpétue la spirale. C'est pourquoi de nombreux patients atteints de MICI souffrent de diverses formes d'arthrite, notamment d'arthrose, de rhumatisme psoriasique, etc. L'inflammation systémique peut parfois se manifester par des maladies pulmonaires, cardiaques, rénales, cérébrales ou hépatiques associées aux MICI, voire par des cancers.
Processus de réparation
Par le biais d'un mécanisme de communication intercellulaire connu sous le nom d'effet paracrine, les ADRC mobilisent les cellules voisines pour qu'elles travaillent plus efficacement. Elles recrutent les services biologiques d'incendie, de secours et de réparation du site - les cellules souches résidentes - pour qu'ils se remettent au travail et fassent leur part.
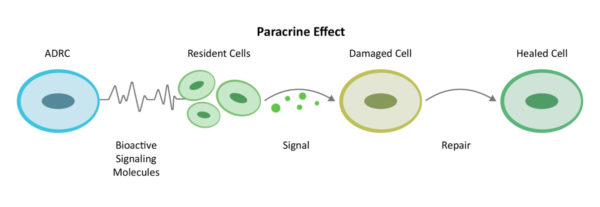
En recrutant d'autres "réparateurs" sur le site (cellules souches résidentes) pour qu'ils reprennent le travail et fassent leur part, les ADRC forment une équipe élargie et travaillent d'abord à la réduction de l'inflammation et des réponses immunitaires hyperactives. Une fois que la conduite sur la banquette arrière diminue, ils poursuivent leur travail en augmentant la circulation grâce à la croissance de nouveaux vaisseaux sanguins, en empêchant toute nouvelle mort cellulaire, en s'attaquant au tissu cicatriciel et en régénérant les tissus sains et les nerfs. C'est ainsi que le corps guérit naturellement, mais si l'insulte causée par une affection aiguë ou chronique est trop importante, il a besoin d'aide.
C'est ce que nous appelons le processus de réparation. Il implique les multiples mécanismes d'action nécessaires pour rééquilibrer l'inflammation systémique et la réponse immunitaire.
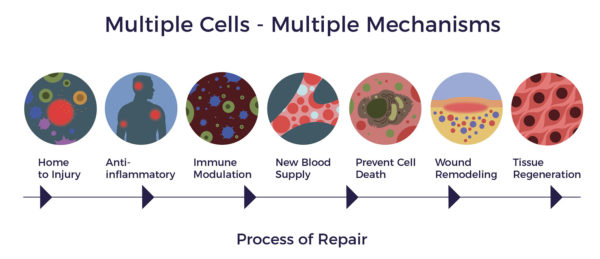
Le processus peut s'étendre aux conditions arthritiques associées ainsi qu'aux organes affectés par les maladies inflammatoires de l'intestin.
Les cellules souches ont des propriétés régénératrices et modulatrices sur le système immunitaire, ce qui conduit à la réduction de l'inflammation et à la guérison des tissus intestinaux affectés.[7] Des études sur l'homme ont montré que les cellules souches infusées par voie veineuse réduisaient de manière significative la maladie de Crohn et la colite ulcéreuse, une étude faisant état de 68% de patients capables d'arrêter les stéroïdes après la thérapie cellulaire. [8] [9] Une rémission de longue durée a été obtenue chez certains patients.[10]
Les cellules souches sont bien connues pour leur capacité à cicatriser les plaies et, dans des études humaines, il a été démontré que les cellules souches fermaient les fistules associées à la maladie de Crohn. [11] [12] [13] [14] [15] et de résoudre l'inflammation dans le canal de la fistule. [16] [17]
Thérapie cellulaire AMBROSE pour les maladies inflammatoires de l'intestin
La thérapie cellulaire AMBROSE représente une option peu invasive pour améliorer les symptômes, la fonction et la qualité de vie des patients souffrant de maladies inflammatoires de l'intestin. Des plans de traitement personnalisés sont élaborés pour chaque patient, en tenant compte de la structure, de la biologie et de l'état médical de chacun.
S'il vous plaît nous contacter pour plus d'informations sur le traitement, la candidature et la procédure à suivre pour devenir patient.
[1]JK Fraser PhD et S. Kesten MD Autologous Adipose Derived Regenerative Cells : Une plateforme pour des applications thérapeutiques Cicatrisation avancée des plaies Technologie chirurgicale internationale XXIX
[2] A Nguyen, A et al Stromal vascular fraction : Une réalité régénératrice ? Part 1 : Current concepts and review of the literature Journal of Plastic, Reconstructive & Aesthetic Surgery (2016) 69, 170e179.
[3] Guo et al Stromal vascular fraction : Une réalité régénératrice ? Part 2 : Current concepts and review of the literature Journal of Plastic, Reconstructive & Aesthetic Surgery (2016) 69, 180e188
[4] F. De Francesco et al Le rôle des cellules souches adipeuses dans les maladies inflammatoires de l'intestin : De la biologie aux nouvelles stratégies thérapeutiques CANCER BIOLOGY & THERAPY 2016, VOL. 17, NO. 9, 889-898
[5] Qui et al Revue systématique avec méta-analyse : l'efficacité et la sécurité de la thérapie par cellules souches pour la maladie de Crohn Stem Cell Research & Therapy (2017) 8:136.
[6] C. Franceschi and J. Campisi Chronic Inflammation (Inflammaging) and Its Potential Contribution to Age-Associated Diseases J Gerontol A Biol Sci Med Sci 2014 June;69(S1) : S4-S9
[7] Dave M, Mehta K, Luther J, Baruah A, Dietz AB, Faubion WA. Thérapie par cellules souches mésenchymateuses pour les maladies inflammatoires de l'intestin : A Systematic Review and Meta-analysis. Inflamm Bowel Dis. 2015;21(11):2696–2707
[8] Lazebnik LB, Konopliannikov AG, Kniazev OV, et al [Utilisation de cellules souches mésenchymateuses allogènes dans le traitement des maladies inflammatoires intestinales] Ter Arkh. 2010;82:38-43
[9] Forbes GM, Sturm MJ, Leong RW, et al. A phase 2 study of allogeneic mesenchymal stromal cells for luminal Crohn's disease refractory to biologic therapy. Clin Gastroenterol Hepatol. 2014;12:64-71
[10] Liang J, Zhang H, Wang D, et al. Allogeneic mesenchymal stem cell transplantation in seven patients with refractory inflammatory bowel disease. Gut. 2012;61:468-469
[11] Garcia-Olmo D, Garcia-Arranz M, Garcia LG, et al. Autologous stem cell transplantation for treatment of rectovaginal fistula in perianal Crohn's disease : a new cell-based therapy. Int J Colorectal Dis. 2003;18:451-454
[12] Garcia-Olmo D, Garcia-Arranz M, Herreros D, et al. A phase I clinical trial of the treatment of Crohn's fistula by adipose mesenchymal stem cell transplantation. Dis Colon Rectum. 2005;48:1416-1423
[13] Garcia-Olmo D, Herreros D, Pascual I, et al. Expanded adipose-derived stem cells for the treatment of complex perianal fistula : a phase II clinical trial. Dis Colon Rectum. 2009;52:79-86
[14] Cho YB, Lee WY, Park KJ, et al. Autologous adipose tissue-derived stem cells for the treatment of Crohn's fistula : a phase I clinical study. Cell Transplant. 2013;22:279-285
[15] Lee WY, Park KJ, Cho YB, et al. Autologous adipose tissue-derived stem cells treatment demonstrated favorable and sustainable therapeutic effect for Crohn's fistula. Stem Cells. 2013;31:2575-2581
[16] Ciccocioppo R, Bernardo ME, Sgarella A, et al. Autologous bone marrow-derived mesenchymal stromal cells in the treatment of fistulising Crohn's disease. Gut. 2011;60:788-798
[17] de la Portilla F, Alba F, Garcia-Olmo D, et al. Expanded allogeneic adipose-derived stem cells (eASCs) for the treatment of complex perianal fistula in Crohn's disease : results from a multicenter phase I/IIa clinical trial. Int J Colorectal Dis. 2013;28:313-323
